Un partenariat novateur pour encadrer les thérapies numériques en santé mentale
La santé mentale est de plus en plus au cœur des préoccupations, une initiative britannique novatrice pourrait bien optimiser l'approche des thérapies numériques en santé mentale. L'Agence britannique de réglementation des médicaments et des produits de santé (MHRA) et l'Institut national pour l'excellence en santé et en soins (NICE) unissent leurs forces dans un projet ambitieux visant à encadrer et évaluer ces outils prometteurs. Cette collaboration, financée à hauteur de 1,8 million de livres sterling par Wellcome, ouvre la voie à une utilisation plus sûre et plus efficace des technologies numériques, tout en favorisant l'innovation dans un domaine en pleine expansion.

Dans un contexte où la demande de services de santé mentale dépasse largement les ressources disponibles à l’échelle mondiale, les thérapies numériques en santé mentale (TDNSM) émergent comme une solution prometteuse pour réinventer la prestation de soins en santé mentale. Comme le soulignent Hopkin et ses collègues, ces technologies offrent des approches innovantes, efficaces et personnalisées qui peuvent répondre aux préférences et objectifs individuels des patients.
Cependant, le développement rapide des TDNSM soulève également de nouveaux défis en termes de sécurité et d’efficacité. C’est dans ce contexte que l’Agence britannique de réglementation des médicaments et des produits de santé (MHRA) et l’Institut national pour l’excellence en santé et en soins (NICE) ont lancé un partenariat ambitieux. Financé par Wellcome à hauteur de 1,8 million de livres sterling, ce projet sur trois ans vise à développer des approches robustes pour la réglementation et l’évaluation des TDNSM.
Débuté en mai 2023, ce partenariat répond aux appels des parties prenantes pour plus de clarté dans ce domaine en pleine expansion. Il cherche à garantir que les TDNSM sont sûres, efficaces et bénéfiques pour les patients, tout en favorisant l’innovation. Les auteurs soulignent l’importance d’impliquer les patients, le public et les professionnels de la santé mentale dans ce processus pour s’assurer que les approches de réglementation et d’évaluation sont éclairées par leurs perspectives.
Les défis clés abordés par le projet
Définir l’objectif et la classification des TDNSM
Un défi majeur identifié par Hopkin et ses collègues est la nécessité pour les développeurs de fournir une description claire et précise de l’objectif visé par leur technologie numérique en santé mentale (TDNSM). L’Agence britannique de réglementation des médicaments et des produits de santé (MHRA) recommande que cette description inclue le fonctionnement de la TDNSM, ses buts, ses utilisateurs cibles et son environnement d’utilisation.
Pour élaborer cette description détaillée, les développeurs doivent s’engager précocement auprès des adopteurs potentiels et des utilisateurs finaux. Cette collaboration est essentielle pour comprendre comment intégrer leurs technologies dans les systèmes existants et identifier les éventuelles modifications nécessaires des parcours de soins pour faciliter l’adoption.
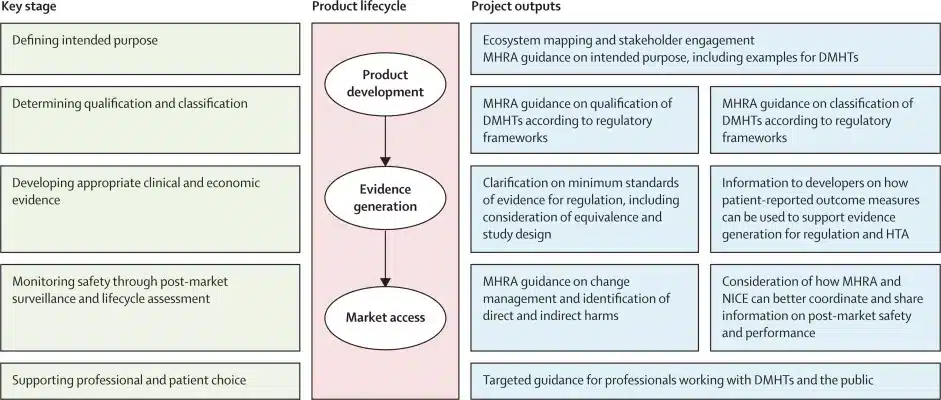
Les auteurs soulignent que, selon leur expérience, de nombreuses descriptions d’objectifs pour les TDNSM sont actuellement inadéquates. De plus, ces descriptions peuvent devenir inexactes lorsqu’un développeur élargit l’objectif de sa technologie sans mettre à jour la documentation correspondante, ce qui peut avoir des conséquences importantes sur les utilisateurs et les risques associés.
Un autre défi majeur concerne la classification des TDNSM comme dispositifs médicaux. Bien que la MHRA fournisse des directives sur la qualification et la classification des logiciels en tant que dispositifs médicaux, ces directives ne comprennent pas d’exemples spécifiques pour la santé mentale. Cette lacune rend les jugements particulièrement difficiles, car de nombreuses TDNSM ciblent des symptômes liés à la santé mentale (comme le sommeil, l’humeur ou le stress) sans nécessairement traiter des conditions médicales à proprement parler.
Établir des normes de preuves adaptées
Le projet vise également à définir les preuves cliniques et économiques nécessaires pour démontrer la sécurité et l’efficacité des TDNSM. Hopkin et ses collègues soulignent l’importance de trouver un équilibre entre la rigueur scientifique et la facilitation de l’innovation dans ce domaine en pleine expansion.
Le NICE publiera des recommandations sur l’utilisation de certaines TDNSM au sein du NHS en se basant sur leur efficacité et leur rapport coût-efficacité par rapport aux soins établis. Cependant, les auteurs notent que de nombreuses TDNSM pourraient ne pas disposer de preuves cliniques ou économiques suffisantes pour répondre aux exigences réglementaires ou pour que le NICE recommande leur utilisation routinière.
Bien que le NICE ait développé un cadre de normes de preuves pour les technologies de santé numériques, les auteurs soulignent qu’une plus grande clarté est nécessaire sur la classification des TDNSM au sein de ce cadre. Ils suggèrent également que des détails supplémentaires pourraient être fournis sur des aspects spécifiques de la conception d’études de haute qualité, comme les méthodes quasi-expérimentales appropriées et les mesures de résultats rapportées par les patients les plus pertinentes.
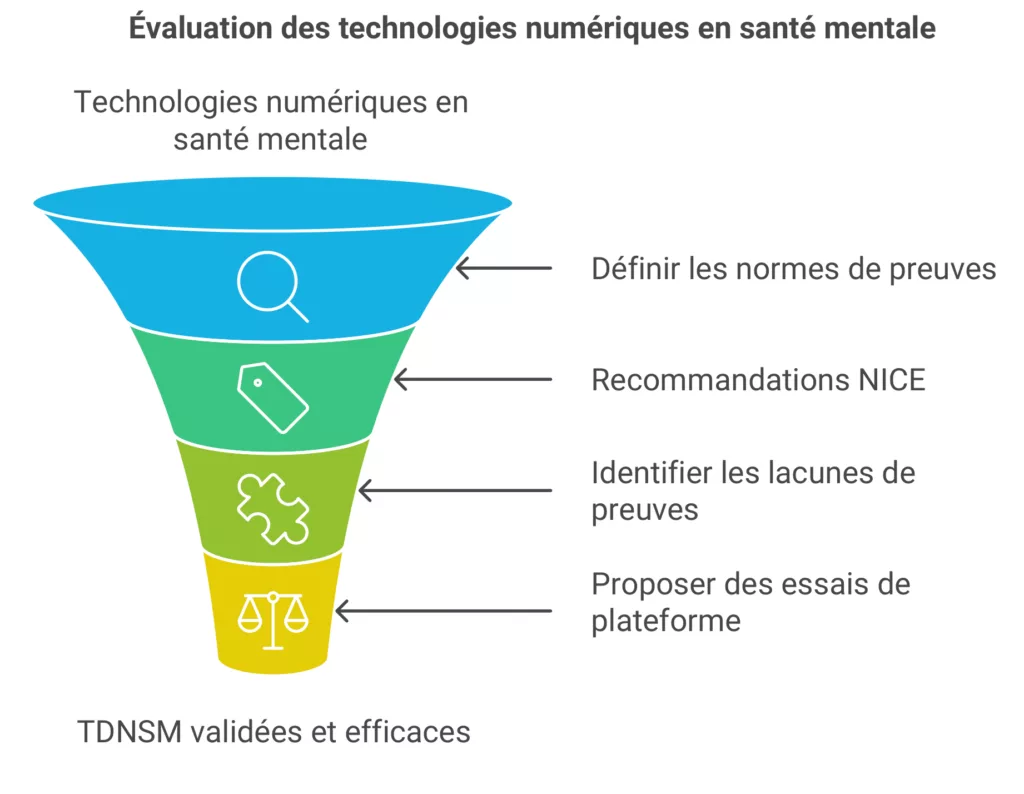
Les auteurs évoquent également la possibilité d’explorer des approches innovantes pour développer des preuves, comme les essais de plateforme. Ces essais, grâce à leur conception adaptative, permettraient d’évaluer les TDNSM dans le temps et de les comparer simultanément à plusieurs interventions de référence.
Assurer un suivi post-commercialisation efficace
La surveillance des TDNSM après leur mise sur le marché est un aspect crucial identifié par Hopkin et ses collègues. En 2023, la MHRA a publié des directives sur le signalement des incidents indésirables impliquant les logiciels en tant que dispositifs médicaux (SaMD) via des systèmes de vigilance, incluant des références aux préjudices directs et indirects liés à l’utilisation des TDNSM.
Le projet explore comment renforcer ces systèmes de signalement et exploiter de nouvelles sources de données. Les auteurs suggèrent que les nouvelles approches du NICE, recommandant la génération de preuves pendant l’utilisation des TDNSM dans des contextes réels, pourraient compléter ces mécanismes de retour d’information.
Plusieurs pistes sont envisagées :
– L’utilisation de données collectées en routine après l’adoption pour soutenir la surveillance en conditions réelles.
– Des approches novatrices pour surveiller les avis sur les produits dans les magasins d’applications et autres forums.
– L’intégration potentielle des données collectées lors des interactions avec les TDNSM dans les ensembles de résultats.
Cependant, ces approches présentent également des défis pratiques, comme la nécessité de s’assurer que l’utilisation des TDNSM est correctement codée dans les dossiers des patients.
Guider les utilisateurs dans le choix des TDNSM
Face à la multiplication des TDNSM disponibles pour le public, les patients et les professionnels de santé, le projet vise à fournir des conseils adaptés à chacun de ces groupes. L’objectif est de les aider à comprendre les défis réglementaires et d’évaluation mentionnés précédemment, et de les soutenir dans le choix de produits sûrs et efficaces répondant à leurs besoins.
Cette orientation est particulièrement importante compte tenu de la croissance rapide du marché des TDNSM et de la diversité des technologies disponibles, allant des applications simples aux systèmes plus complexes utilisant l’intelligence artificielle générative.
Une approche collaborative et internationale
Le projet MHRA-NICE adopte une démarche collaborative, impliquant de nombreuses parties prenantes. Les auteurs soulignent l’importance d’impliquer les patients, le public et les professionnels de la santé mentale dans ce processus pour s’assurer que les approches de réglementation et d’évaluation sont éclairées par leurs perspectives.
La dimension internationale est également prise en compte. Le MHRA est membre du Forum international des régulateurs des dispositifs médicaux, qui vise à renforcer l’harmonisation et la convergence réglementaires.
À travers ce projet et d’autres initiatives de recherche et de collaboration, le MHRA et le NICE s’engagent auprès des régulateurs internationaux et des agences d’ETS pour partager les enseignements et explorer une harmonisation internationale plus poussée.Le projet vise également à explorer comment les pays dotés de voies réglementaires moins établies peuvent développer des cadres permettant un accès sûr aux TDNSM.
Les enjeux pour l’avenir des TDNSM
L’avenir des technologies numériques en santé mentale (TDNSM) repose sur plusieurs enjeux clés, comme le soulignent Hopkin et ses collègues. Tout d’abord, il est essentiel d’assurer que ces technologies soient non seulement innovantes, mais également sûres et efficaces. La MHRA et le NICE travaillent ensemble pour établir un cadre réglementaire qui répond aux besoins des utilisateurs tout en soutenant l’innovation. Cela implique de clarifier les exigences réglementaires et d’évaluation pour les TDNSM, afin que les développeurs comprennent ce qui est attendu d’eux.
Ensuite, la question de la preuve d’efficacité et de sécurité reste centrale. Les TDNSM doivent fournir des données cliniques et économiques solides pour justifier leur utilisation dans les soins de santé. Le NICE a déjà mis en place un programme d’évaluation précoce pour intégrer rapidement les technologies prometteuses dans le système de santé. Cependant, il existe encore un besoin urgent de normes claires concernant les types de preuves requises pour différentes catégories de TDNSM.
Enfin, l’intégration des TDNSM dans les parcours de soins existants pose également un défi. Les technologies doivent être conçues non seulement pour répondre aux besoins des patients, mais aussi pour s’intégrer harmonieusement dans les systèmes de santé en place. Cela nécessitera une collaboration étroite entre développeurs, professionnels de santé et régulateurs pour garantir que les TDNSM soient adoptées efficacement et qu’elles apportent une réelle valeur ajoutée aux soins.
Les implications pour la France et l’Europe
Bien que le projet MHRA-NICE soit basé au Royaume-Uni, ses résultats pourraient avoir des répercussions significatives en France et dans toute l’Europe. De nombreux pays européens font face à des défis similaires concernant la réglementation des TDNSM. Les approches développées dans le cadre de ce projet pourraient inspirer des initiatives similaires sur le continent.
En France, où la santé mentale est une grande cause nationale 2025, la réglementation des TDNSM pourrait bénéficier d’un cadre similaire à celui proposé par la MHRA et le NICE. L’intégration des perspectives des utilisateurs finaux est cruciale pour garantir que ces technologies répondent aux besoins réels des patients. En impliquant activement les patients et le public dans le processus de développement et d’évaluation, la France pourrait améliorer l’acceptabilité et l’efficacité des TDNSM.
De plus, la coopération entre les agences réglementaires européennes pourrait faciliter l’harmonisation des normes d’évaluation et de réglementation. Cela permettrait non seulement d’accélérer l’accès aux TDNSM sûres et efficaces sur le marché européen, mais aussi de renforcer la confiance du public dans ces technologies.
Vers une nouvelle ère pour les TDNSM
Le projet MHRA-NICE marque une étape importante dans l’encadrement des technologies numériques en santé mentale. En développant un cadre réglementaire clair et adapté, ce partenariat vise à garantir que ces outils innovants soient non seulement sûrs et efficaces, mais aussi accessibles aux patients qui en ont besoin.
Pour réaliser le potentiel des TDNSM, il est impératif que tous les acteurs — développeurs, régulateurs, professionnels de santé et utilisateurs — collaborent étroitement. L’inclusion significative des personnes ayant une expérience vécue dans le processus de développement est essentielle pour s’assurer que ces technologies répondent aux attentes et aux besoins réels.
À mesure que ce projet avance vers sa conclusion prévue en 2026, il ouvrira sans aucun doute la voie à une utilisation plus sûre et plus efficace des TDNSM dans le monde entier. En favorisant l’innovation tout en garantissant la sécurité, cette initiative pourrait transformer radicalement la manière dont les soins en santé mentale sont fournis, améliorant ainsi la qualité de vie de millions de personnes souffrant de troubles mentaux.
Source : The Lancet Digital Health, 15 November 2024
Building robust, proportionate and timely approaches to the regulation and evaluation of digital mental health technologies
∙ Richard Branson, MAb ∙ Paul Campbell, FRCAb ∙ Holly Coole, PgDipb ∙ Sophie Cooper, BSca ∙ Francesca Edelmann, BScb ∙ Grace Gatera, BAc ∙ Jamie Morgan, MAc ∙ Mark Salmon, MBAa


